XƏBƏRLƏR
Курение и кожа

Абстракт | Курение сигарет неразрывно связано с серьезной патологией всех систем организма человека, и кожные покровы — не исключение. Предмет этого обзора — вред, который приносит коже потребления табака. Важно определить разницу между эффектами табакокурения и собственным влиянием никотина на кожу. Все клетки кожи экспрессируют несколько подтипов никотиновых ацетилхолиновых рецепторов (нХР), включая рецептор подтипа α7. На одни хронические дерматозы курение влияет отрицательно, на другие — положительно. Выявив отрицательное влияние курения на определенное заболевание, пациентам можно рекомендовать отказ от курения, а в противоположных случаях — разработать терапевтические агенты на основе агонистов нХР.
Токсичные составляющие табачных изделий
Курение сигарет неразрывно связано с серьезной патологией всех систем организма человека, и кожные покровы — не исключение. Несмотря на попытки предостеречь население от опасностей курения, оно сохраняет лидирующие позиции в качестве одной из причин предотвратимой смертности. Табакокурение известно в Европе с тех пор, как Христофор Колумб в 1492 г. заметил, как индейцы Араваки курили листья табака. Растение табака назвали Nicotiana tabacum в честь французского посла в Португалии, который приобщил Францию к этому растению — Жана Нико (Jean Nicot). Никотин — основной алкалоид табака — был выделен в 1828 г. Никотин может проникать в организм человек при попадании дыма в легкие или желудочно-кишечный тракт, а также в составе интраназальных спреев, трансдермальных пластырей, кремов для местного применения или клизм. Небольшие количества никотина обнаруживаются в пищевых продуктах, таких как помидоры, картофель и баклажан. Никотин может всасываться в кровоток через ротовую полость, легкие, мочевой пузырь, желудочно-кишечный тракт и через кожу. От 70 до 80 % никотина, всасывающегося в желудочно-кишечном тракте, при первом прохождении через печень превращается в его наиболее важный метаболит — котинин [1]. Скорость всасывания никотина через кожу и слизистые находится в прямой зависимости от его концентрации. Период полувыведения никотина составляет приблизительно два часа [2].
С точки зрения дерматологии употребление табака несет в себе много опасностей для кожи, которые могут реализоваться как через прямое влияние на эпидермис, так и опосредованно — через кровоток. Табачный дым состоит из твердой дисперсной фазы, к которой относится и его основной алкалоид — никотин, а также летучей фазы. В табачном дыму много мутагенов и канцерогенов, в частности, полициклические ароматические углеводороды (ПАУ), нитрозамины и гетероциклические амины. Основные токсические компоненты твердой фазы включают в себя никотин, фенол, катехол, хинолин, анилин, толуидин, никель, N-нитрозодиметиламин, бензапирены, бензантрацен и 2-нафтиламин. Основные токсические компоненты газовой фазы — углекислый газ, угарный газ, циановодород, оксид азота, ацетон, формальдегид, акролеин, катионы аммония, пиридин, 3-винилпиридин, N-нитрозодиметиламин и N-нитрозопирролидин. Исследования экспрессии генов в клетках кожи показали, что компоненты табака активируют экспрессию 14 различных генов, участвующих в метаболизме ксенобиотиков и ответе на окислительной или иной стресс [3]. Негеномные эффекты табачного дыма обусловлены образованием активных форм кислорода (АФК). Никотин и его метаболиты влияют на кожу посредством активации никотиновых холинорецепторов (нХР), экспрессируемых эпителиоцитами [4].
Признаки курения на слизистых оболочках и коже
Заядлых курильщиков, как правило, можно определить по характерным проявлениям на коже и слизистых оболочках. Часто обнаруживают желтое окрашивание светлых усов и ногтей, пропитанных побочными продуктами табака. При прекращении курения между дистальной пигментированной частью ногтя и растущим нормальным ногтем появляется различимая граница — явление, известное как ноготь Арлекина или ноготь «бросающего» (Рис. 1). По длине выросшего нормального ногтя можно предположить, как долго человек не курит. Хроническое нагревание от зажженной сигареты также окрашивает кончики пальца за счет пост-воcпалительной гиперпигментации. У одной трети курильщиков заметна периоральная гиперпигментация [5]. У детей, пассивно вдыхающих табачный дым [6], а также употребляющих никотин сублингвально, можно обнаружить пигментацию десен [7]. Пигментация десен обусловлена образованием гранул меланина, синтезирующихся в меланосомах. Никотин, который может выступать предшественником синтеза меланина, способен необратимо связываться с меланином и накапливаться в меланин-содержащих тканях [8]. Известно, что и другие компоненты табака, в особенности такие канцерогены, как N`-нитрозонорникотин (NNN), 4-(метилнитрозамино)-1-(3-пиридил)-1-бутанон (NNK) и бензапирен, накапливаются в тканях, содержащих меланин [9].
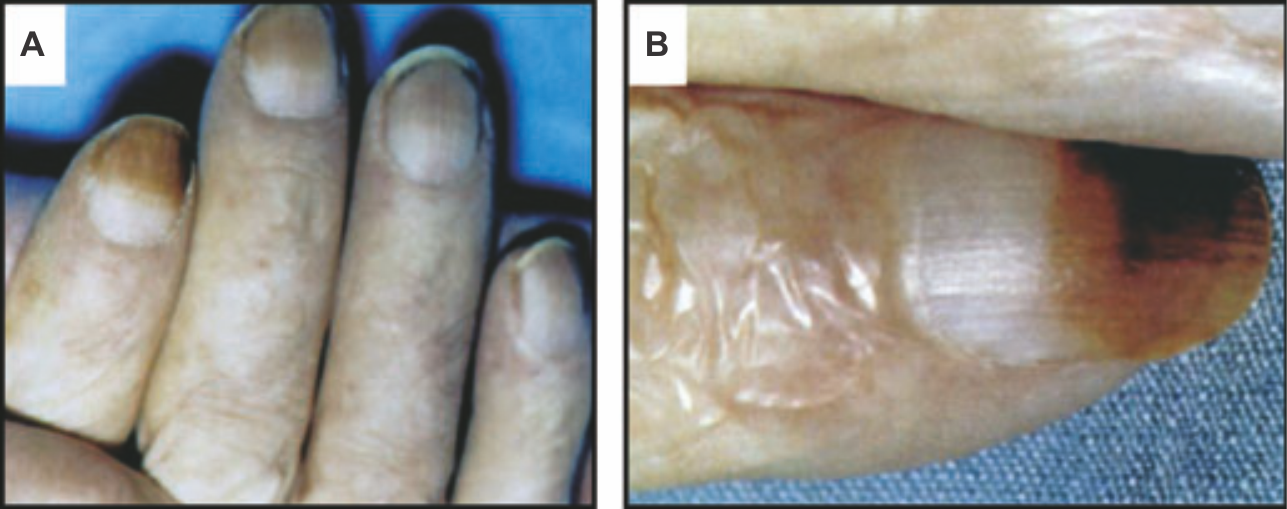
Таблица 1 | Обобщенные эффекты табака/никотина на кожу
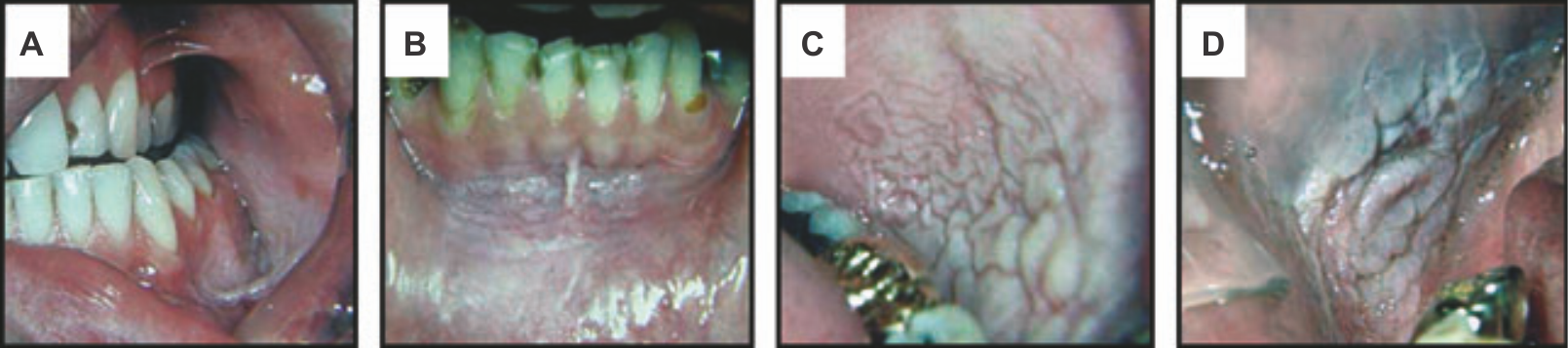
Курение может оказывать влияние и на язык, небо и другие анатомические образования ротовой полости. У курильщиков можно обнаружить характерную гиперплазию сосочков и черную пигментацию дорсальной поверхности языка, т. н. «черный волосатый» язык. Язык курильщика (или никотиновая лейкоплакия языка, leukokeratosis nicotina glossi) — однородный кератоз с воспаленными слюнными железами, которые выглядят как папулы с углублением по середине. У курильщиков биди (табака, завернутого в лист Кромандельского черного дерева) встречается центральная атрофия сосочков языка, обратимая при прекращении курения. Небо курильщика (или никотиновая лейкоплакия неба, leukokeratosis nicotina palati) — бессимптомный однородный кератоз задних двух третей твердого неба в сочетании с множественными красными вдавленными по середине папулами, представляющими собой воспаленные слюнные железы. Встретить такое можно исключительно у курильщиков, особенно у заядлых любителей трубки. С другой стороны, у любителей пожевать табак появляется белое окрашивание в месте соприкосновения с табаком, которое может изъязвляться (Рис. 2)
Преждевременное старение кожи
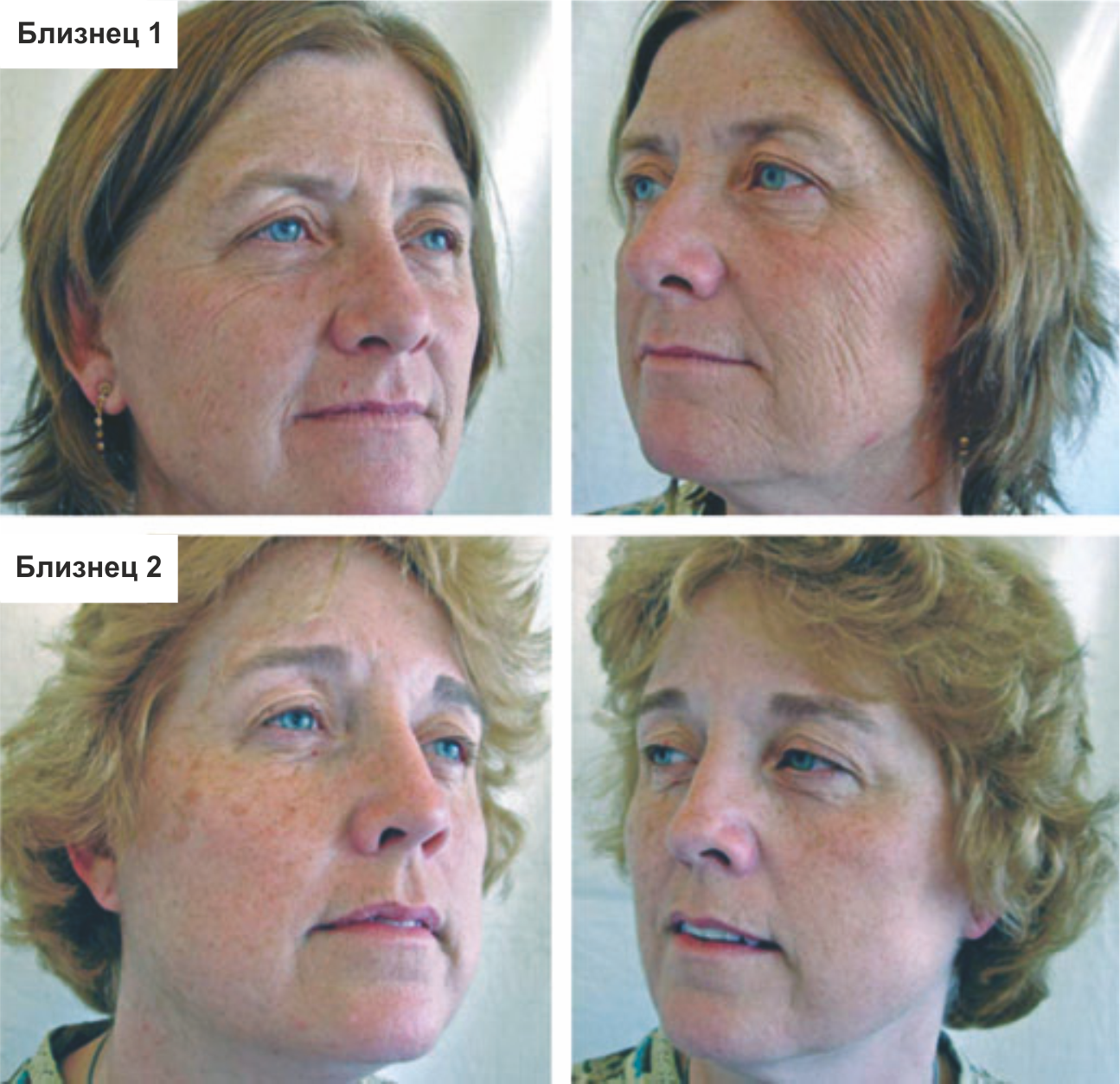
Одно из наиболее характерных и общественно значимых проявлений курения — преждевременное старение. «Лицо курильщика» типично испещрено выраженными морщинами, черты лица истончаются, подчеркивая костный рельеф, кожа атрофичная с сероватым оттенком на фоне полнокровия [10]. Степень изменений напрямую связана с количеством выкуриваемых за день сигарет (Рис. 3).
У женщин преждевременное старение выражено сильнее, чем у мужчин. Выраженность морщин усиливается за счет прямого контакта с сигаретным дымом, который высушивает роговой слой эпидермиса и вызывает умеренную воспалительную реакцию [12]. Эксперименты на мышах in vivo также показывают, что пассивное воздействие табачного дыма приводит к преждевременному старению кожи [13]. Кожа, которая подвергается влиянию табачного дыма, тонкая и хрупкая, склонна провисать. В то время как табакокурение само по себе является независимым фактором риска образования морщин, инсоляция усиливает этот эффект [14]. Курение поражает и закрытую от солнца кожу. Наилучшими предикторами степени старения являются количество сигарет, выкуриваемых в день, и возраст.
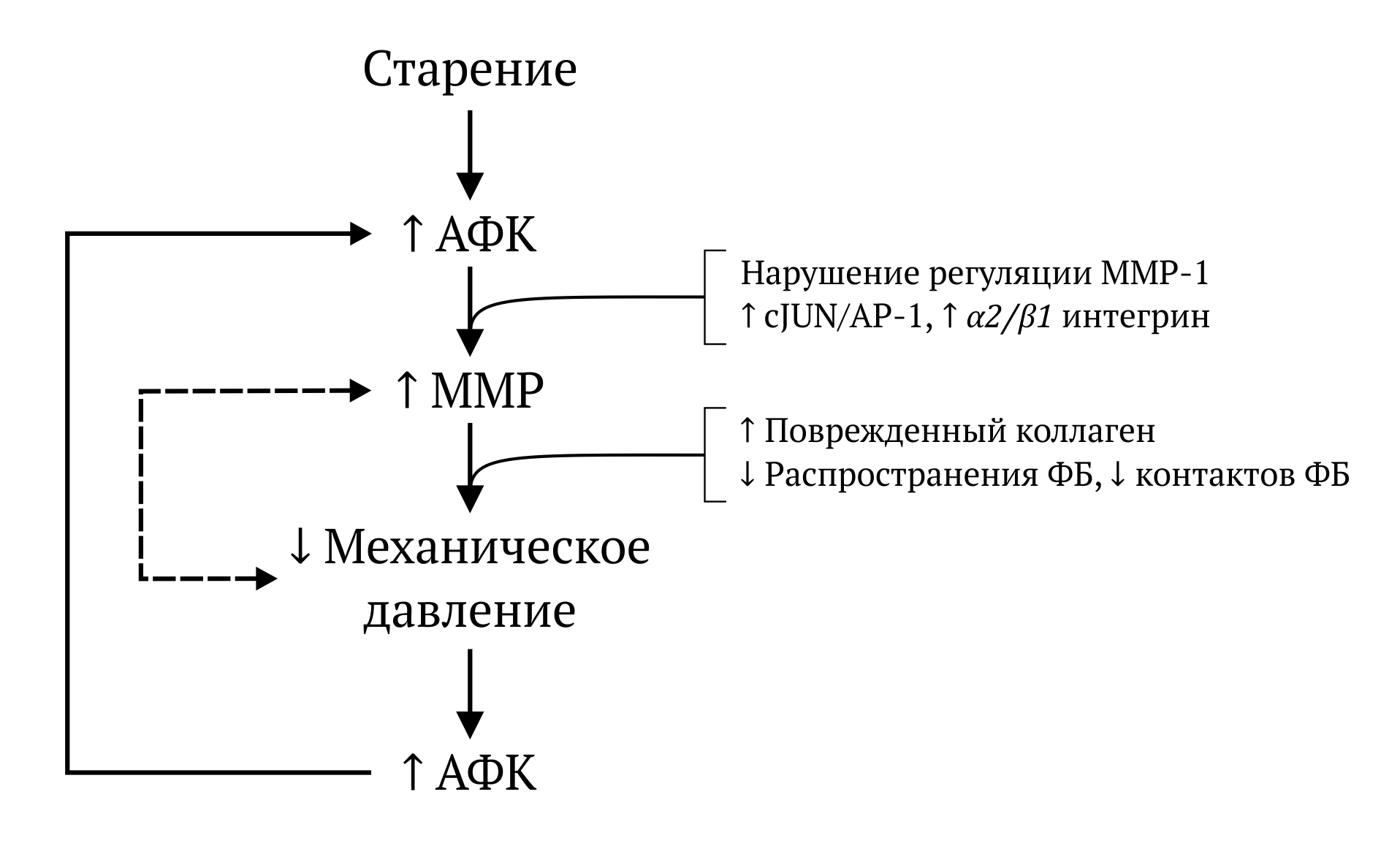
Сигаретный дым — важный фактор ускорения процессов старения за счет образования свободных радикалов и развития соответствующих патологических процессов (Рис. 4). Курение может приводить к изнашиванию механизмов клеточной защиты и репарации, что ведет к накоплению повреждений, связанных с мутациями и дефектными белками. Курение также нарушает обновление межклеточного вещества в коже [17], что приводит к дисбалансу между процессами синтеза и деградации белков соединительной ткани дермы. Помимо того, что курение снижает синтез коллагенов типа I и III (важное условие ускоренного старения кожи) [18], оно также увеличивает содержание тропоэластина и ускоряет деградацию коллагена [19]. Курение — самостоятельный фактор риска увеличения количества эластических волокон сосочкового слоя дермы в коже, не подверженной прямому контакту. Такой прирост — следствие нарастающей деградации эластического вещества, аналогично солнечному эластозу [20].
Нарушения в межклеточном веществе соединительной ткани могут вносить свой вклад в молекулярные механизмы преждевременного старения кожи у курильщиков. Эксперименты in vitro показывают, что биосинтез коллагена в культуре фибробластов значительно снижается после воздействия экстракта табачного дыма [18]. Курение повышает экспрессию металлопротеиназ матрикса (MMP-1, MMP-2, MMP-3, MMP-7, and MMP-8) [17,19]. В коже курильщиков по сравнению с некурящими повышена экспрессия MMP-8, а TIMP-1 — ингибитора MMP, — снижена. Повышенная экспрессия MMP-1 у активных курильщиков определяется и в закрытых от солнца участках кожи. Эксперименты in vitroпоказали, что экстракт табачного дыма может усиливать экспрессию MMP-1 и MMP-3 в фибробластах дермы. Более того, экспрессия MMP-1 существенно увеличивается в фибробластах после стимуляции экстрактом табачного дыма и облучением ультрафиолетом UVA1, вне зависимости от друг друга [18].
Трансформирующий фактор роста (TGF)-b1, вероятно, играет роль в возрастных изменениях кожи, связанных с табакокурением. Табак блокирует ответ клеток на TGF-b, благодаря отрицательной регуляции рецептора TGF-b1 и индукции нефунционирующих его форм, что указывает на роль модуляции TGF-b1 в качестве возможного способа торможения преждевременного старения кожи [22].
Никотин может нарушать ремоделирование дермы за счет увеличения активности регуляторов клеточного цикла, апоптоза и количества коллагена Ia1, эластина и MMP-1 [23]. Изменяя метаболизм межклеточного вещества и экспрессию нХР, он может влиять на физиологическое старение. Никотин также способствует гиперпродукции эластина и гиперэкспрессии нХР-α7 кератиноцитов. Однако никотинергическое влияние на фибробласты дермы в основном опосредовано подтипом нХР-а3 [24].
Рак кожи
В ходе эпидемиологических исследований выявлены как положительные, так и отрицательные взаимосвязи между курением, заболеваемостью и агрессивностью определенных типов рака кожи. Развитие индуцированного курением рака кожи объясняют следующими механизмами: ускоренное старение, мутагенез, стимуляция роста и инвазии опухолевых клеток, неоваскуляризация и ремоделирование стромы. Несмотря на то, что есть исследования, в которых не обнаружили никакой взаимосвязи с курением, [25] большинство работ установили, что курение — независимый фактор риска развития плоскоклеточного рака (ПР), в частности, ПР пениса, вульвы, шейки матки и ануса [26]. Прекращение табакокурения приводит к снижению этих рисков [27]. Курение увеличивает заболеваемость высокоагрессивными формами ПР вульвы и снижает выживаемость. Курящие женщины с генитальными бородавками в 35 раз сильнее подвержены развитию рака вульвы, что предполагает наличие синергии между курением и генитальными бородавками [27]. Также установлена достоверная взаимосвязь злокачественных новообразований ротовой полости с курением [28]. Курение сигарет без фильтра еще больше увеличивает риск [29]. Курящие женщины особенно подвержены ПР ротовой полости [30].
Большинство исследований не нашли четкой ассоциации между курением и риском базально-клеточного рака (БКР) [26], но данные противоречивы. Курение сигарет, возможно, связано с преобладанием больших по размеру БКР (>1 см в диаметре) [31] и более агрессивных форм [32].
Более ранние исследования, в которых изучалась взаимосвязь курения и меланомы, выявили, что количество курящих мужчин в ремиссии через пять лет после постановки диагноза значительно меньше, чем некурящих [33]. У курильщиков выше вероятность раннего и висцерального метастазирования [34]. Более поздние исследования, однако, показывают, что привычка курить никак не влияет на риск злокачественного течения меланомы [26]. Многолетнее курение даже может снизить риск развития меланомы, особенно акральной меланомы [35]. Защитный эффект курения относительно кожной меланомы может быть связан с участием никотина в синтезе меланина, его аффинитетом к меланин-содержащим тканям, необратимым связыванием с меланином и депонированием канцерогенов табака NNK и NNN в тканях, содержащих меланин. Примечательно, что на примере бесшерстных мышей было показано ингибирующее влияние компонентов табака, обусловленное блоком сигнального пути ядерного фактора-jB, на индуцируемые облучением UVB опухоли кожи [13].
Курение связано со сниженным риском классической саркомы Капоши (кСК) [36] и СПИД-ассоциированной саркомой Капоши. Однако в ходе клинических испытаний трансдермальный никотин в лечении кСК у некурящих оказался неэффективным относительно очагов кСК или вирусной нагрузки HHV-8 [38]. Канцерогенность табака в основном связана с действием ПАУ, нитрозаминов и гетероциклических аминов. Известно, что курение замедляет репарацию одноцепочечных разрывов ДНК [39], а также оказывает прямой онкогенный эффект [40]. Проонкогенный эффект никотина также объясняется увеличением частоты митозов клеток базального слоя и появлением гипертрофированных эпителиальных клеток в эпидермисе [41]. Никотин и нитрозамин, содержащиеся в табаке, способствуют росту опухолей благодаря положительной регуляции клеточных нХР, что индуцирует инвазию злокачественных клеток и ингибирует апоптоз [42]. Проинвазивные эффекты никотина обусловлены нХР-α7 [43]. Никотин увеличивает секрецию ацетилхолина, а также экспрессию и активность нХР в злокачественных клетках [44]. Рецептор‑опосредованная токсичность табака — результат взаимодействия нисходящих сигнальных путей Ras/Raf‑1/MEK1/ERK, а также JAK-2/STAT-3, начинающихся с активации нХР‑α7 кератиноцитов (Рис. 5) [45]. Также доказано, что никотин стимулирует рост опухолей за счет увеличения активности phospho-ERK (фосфорилированная киназа, регулируемая внеклеточными сигналами). Пролиферативные эффекты никотина можно предотвратить при помощи высокоаффинного блокатора нХР‑α7 — α‑кобратоксина [46]. Фармакологический блок нХР-α7 растормаживает апоптоз и снижает экспрессию фактора роста эндотелия сосудов (VEGF) — это приводит к ингибированию ангиогенеза [47].
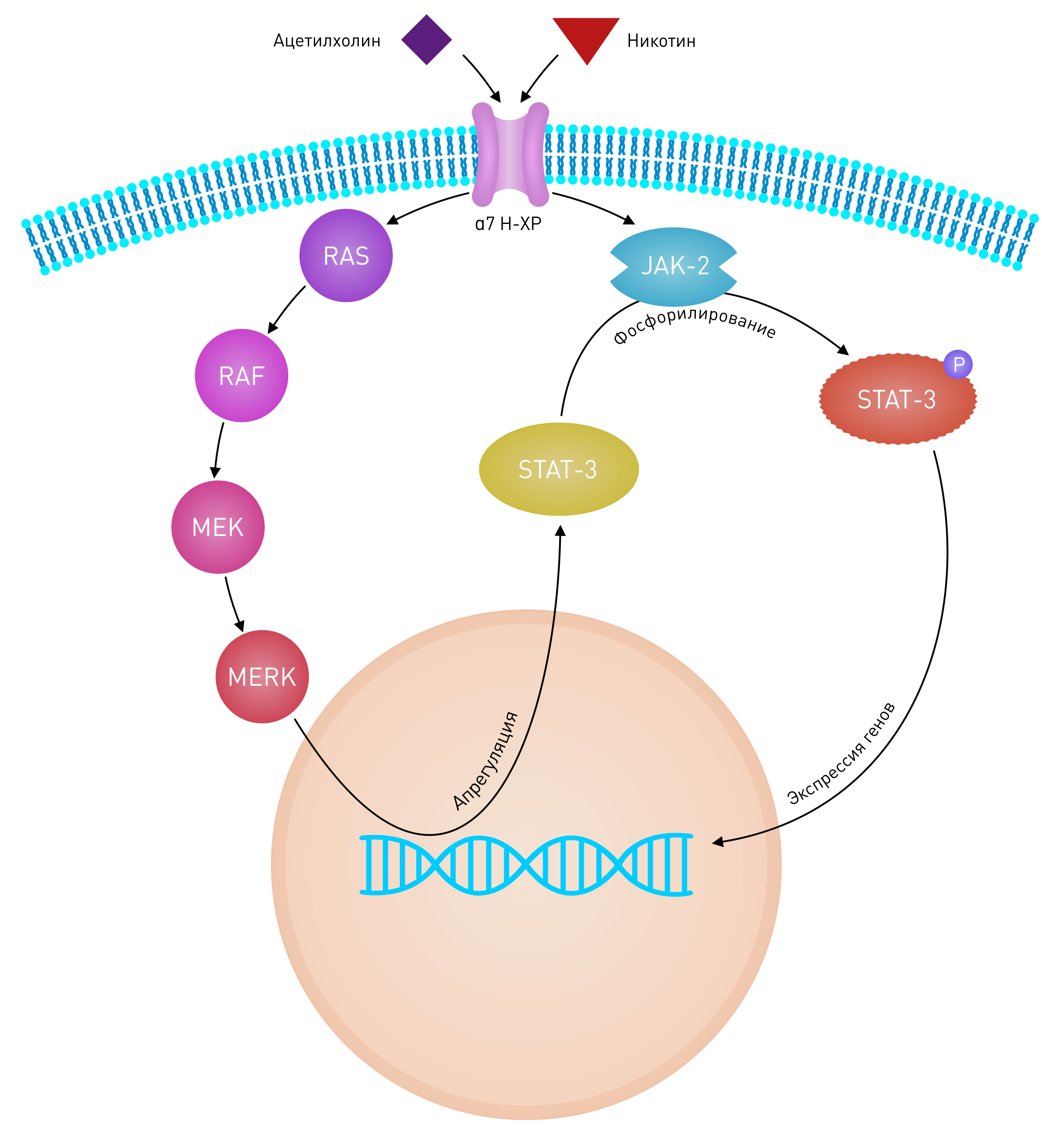
Известны также и непрямые онкогенные эффекты никотина, связанные с эндотелиальными клетками и фибробластами дермы. Никотин может усилить рост опухоли за счет усиления опухолевой васкуляризации и создания про‑канцерогенной среды в строме [49]. Воздействие экстракта бездымного табака на дермальные фибробласты усиливает выработку факторов, ускоряющих пролиферацию и прорастание иммортализированных кератиноцитов. Таким образом, ультрафиолет и нитрозамины табака могут индуцировать канцерогенез, тогда как никотин способствует росту и распространению измененных клеток.
Нарушение заживления ран
У курильщиков повышен риск осложнений операционных ран [50]. Исследования на животных показали, что курение в течение восьми недель до хирургической операции увеличивает вероятность некроза кожного лоскута [51]. В то же время, воздержание от курения снижает вероятность инфекционных осложнений [52].
Патобиологические основы изменения заживления ран под действием табака сходны с таковыми при преждевременном старении кожи. Например, также снижается выработка коллагена и изменяется метаболизм межклеточного вещества с увеличением уровней MMP-8. Показано, что это способствует нарушению процессов регенерации. Вероятно, курение также влияет на заживление ран за счет ингибирования миграции фибробластов к раневому ложу, что ведет к их накоплению по краю раны. Увеличение продолжительности жизни фибробластов одновременно со снижением их миграции может способствовать фиброзированию и чрезмерному рубцеванию [54]. Важно, что эпителизация раны обусловливается миграцией кератиноцитов поверх обнаженной дермы. Миграция кератиноцитов регулируется как никотиновыми, так и мускариновыми подтипами ХР. Ее можно ингибировать при помощи активации нХР-α7, которые ответственны за сопряжение ионных потоков с каскадами протеинкиназных сигнальных путей, регулирующих экспрессию интегрина и активность Rho-киназы [55–58].
Курение может замедлять заживление ран опосредованно через замедление кровотока. В то время, как курение снижает объемный кровоток, концентрацию кислорода и активность аэробного метаболизма в коже, никотин сам по себе увеличивает содержание кислорода в тканях, даже несмотря на сниженный кровоток [59]. Скорее всего, влияние курения на микроциркуляцию обусловлено не воздействием никотина. Вероятно, никотин оказывает влияние на регенерацию только в токсических дозах. В терапевтическом диапазоне, однако, трансдермальный никотин показал себя с другой стороны: он нормализует микрососудистую перфузию кожи пальцев [60] и стимулирует заживление ран и ангиогенез [61]. В эксперименте на мышах никотин значимо способствовал регенерации [62]. Помимо положительной регуляции темпа эпителизации, механизм, вероятно, связан с усиленным синтезом коллагена типа I [63].
Хронические дерматозы, на которые влияет курение
Контактный дерматит
Курение сигарет и употребление нюхательного табака — доказанные факторы риска развития аллергического контактного дерматита. В сигаретах обнаруживают следующие аллергены: какао, ментол, лакрица, канифоль и формальдегид [64]. Курение дозозависимо повышает вероятность положительной накожной пробы на никель [65]. Никотин, сам выступая аллергеном, в кожных пробах может вызывать аллергический или простой контактный дерматит на месте аппликации [66].
Атопический дерматит
Хотя у курящих людей титр IgE в сыворотке значительно выше, чем у некурящих, сведения относительно влияния курения на атопический дерматит противоречивы. В одних исследованиях докладывают, что курение — независимый фактор риска экземы кистей [68]. Однако другие исследования такой взаимосвязи между курением и атопическим дерматитом или экземой кистей не выявили [69].
Псориаз
Хороша известна значительная прямая корреляция между псориазом и курением, зависящая от количества сигарет, выкуриваемых в день [69]. Курение — независимый фактор риска псориаза [70], более опасный у мужчин [71]. Более того, периоды ремиссии после лечения у курильщиков короче [72].
Ладонно-подошвенный пустулез (ЛПП)
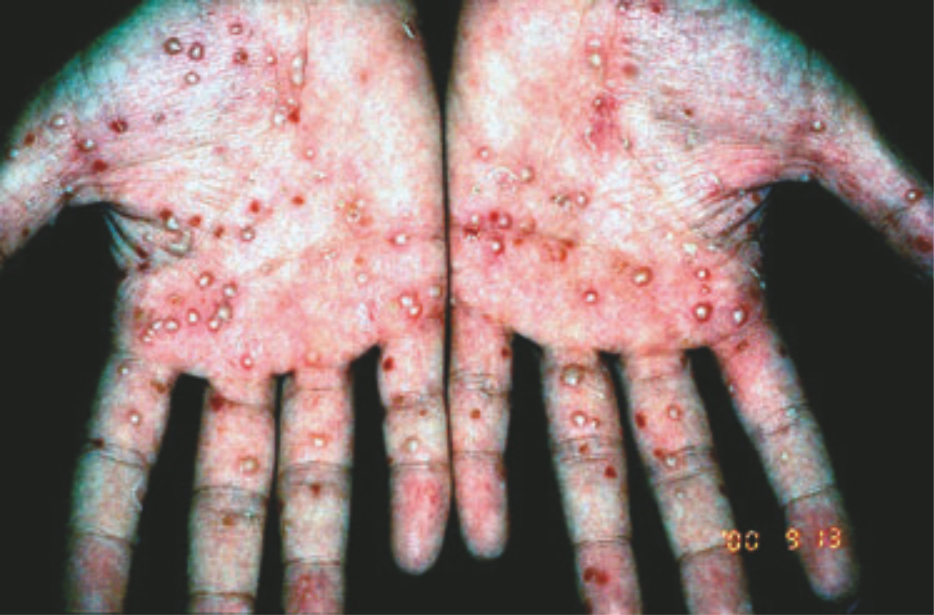
ЛПП (Рис. 6) — одно из наиболее распространенных воспалительных заболеваний кожи, связанное с курением. Около 95 % всех больных ЛПП — курильщики, большинство — заядлые [73]. Прекращение табакокурения значительно улучшает состояние: меньше пустул, меньше площадь эритемы с шелушением [74]. Мишень воспаления при ЛПП — акросирингиум (Интраэпидермальная часть протока потовой железы — прим. ред.). Из-за нарушенной экспрессии нХР и других компонентов холинергической системы кожи у пациентов с ЛПП может развиваться аномальная воспалительная реакция на никотин. Эти наблюдения указывают на роль никотина в
патогенезе ЛПП [75].
Кожная красная волчанка
Исследования выявили статистически значимую связь между активным курением и развитием кожной красной волчанки [76]. Также была показана связь дискоидной красной волчанки (ДКВ) и курения. У курильщиков с ДКВ более обширные поражения при дебюте заболевания [77]. Также эффективность терапии антималярийными препаратами снижается при курении [78].
Болезни волос и волосяных фолликулов
Курение связано с преждевременным поседением волос как у мужчин, так и у женщин, а также с более ранней потерей волос у мужчин [79]. Течение андрогенетической алопеции при частом курении усугубляется, а дебют происходит тем раньше, чем выше доза [80]. Исследования in vivo показали, что у мышей, подвергшихся воздействию табака, развивается атрофия эпидермиса, истончается подкожная жировая клетчатка, количество волосяных фолликулов уменьшается. Также в луковице волоса наблюдается клеточный апоптоз [81]. Курение влияет на микроциркуляторное русло волосяного сосочка в дерме и приводит к повреждению ДНК клеток волосяного фолликула [82]. Оно также выводит из равновесия систему протеаз-антипротеаз, что ведет к изменениям в цикле роста волос. Увеличение концентрации провоспалительных цитокинов вызывает микровоспаление и фиброз фолликулов.
Пустулезные дерматозы
В то время, как одни исследования говорят о дозозависимой линейной связи заболеваемости и тяжести вульгарного акне с табакокурением [83], другие работы такой взаимосвязи не выявили [84]. Напротив, докладывают о более низкой распространенности акне среди курильщиков [85]. Риск развития розацеа среди курильщиков также ниже, вероятно, вследствие сосудосуживающего действия курения [86]. Установлена четкая взаимосвязь курения с гнойным гидраденитом (т. н. инверсные угри) [87]. Ключевым звеном патогенеза гнойного гидраденита, вероятно, выступают холиночувствительные клетки не‑нервного происхождения, о чем говорит аномальная экспрессия нХР в вовлеченной в процесс коже [88].
Пузырные дерматозы
В литературе отмечают, что при курении вульгарная пузырчатка протекает благоприятнее. Это согласуется с данными о том, что среди больных пемфигусом курильщики составляют меньшую часть [89]. Курильщики с вульгарным пемфигусом выходят в частичную и полную ремиссию чаще некурящих [90]. Также существует обратная связь табакокурения с герпетиформным дерматитом и с ассоциированной целиакией [91]. У курильщиков с недавно выявленной целиакией реже обнаруживают антитела к эндомизию, чем у некурящих [92]. Однако в одном исследовании не обнаружили какой-либо взаимосвязи курения с наличием антиглиадиновых антител [93]. Значимой взаимосвязи между курением и пемфигоидом слизистых оболочек не обнаружили [94].
Язвы кожи
Курение — фактор риска развития пролежней [95] и инфицированных язв у пациентов с диабетом [96]. Более 90 % пациентов с язвенными поражениями вследствие болезни Бюргера (облитерирующий тромбангиит) — курильщики. Длительные ремиссии возможны при прекращении табакокурения, тогда как рецидивы обусловлены возвращением ко вредной привычке [97].
Вирусные заболевания кожи
Известно, что курение увеличивает риск возникновения генитальных бородавок у мужчин [98]. А вот заболеваемость заболеваемость рецидивирующим герпесом губ у курильщиков, напротив, значительно ниже, особенно при курении трубки [99]. Скорее всего это связано со способностью табака ингибировать репликацию вируса простого герпеса и значительно снижать его цитолитический эффект [100]. Однако более свежие исследования показали, что аппликации никотина через трансдермальный пластырь индуцируют реактивацию вируса простого герпеса, а также вирусовыделение у кроликов-носителей инфекции [101].
Другие заболевания кожи и слизистых оболочек
Значимая связь установлена между курением и диабетическим липоидным некробиозом [102]. Курение также связывают с генерализованной крапивницей [103]. У мужчин, курящих сигареты или биди, риск развития повреждений кожи, связанных с действием мышьяка, значительно выше, чем у некурящих [104]. С другой стороны, существует обратная связь табакокурения с географическим языком [105].
Заболевания кожи, в лечении которых используют никотин
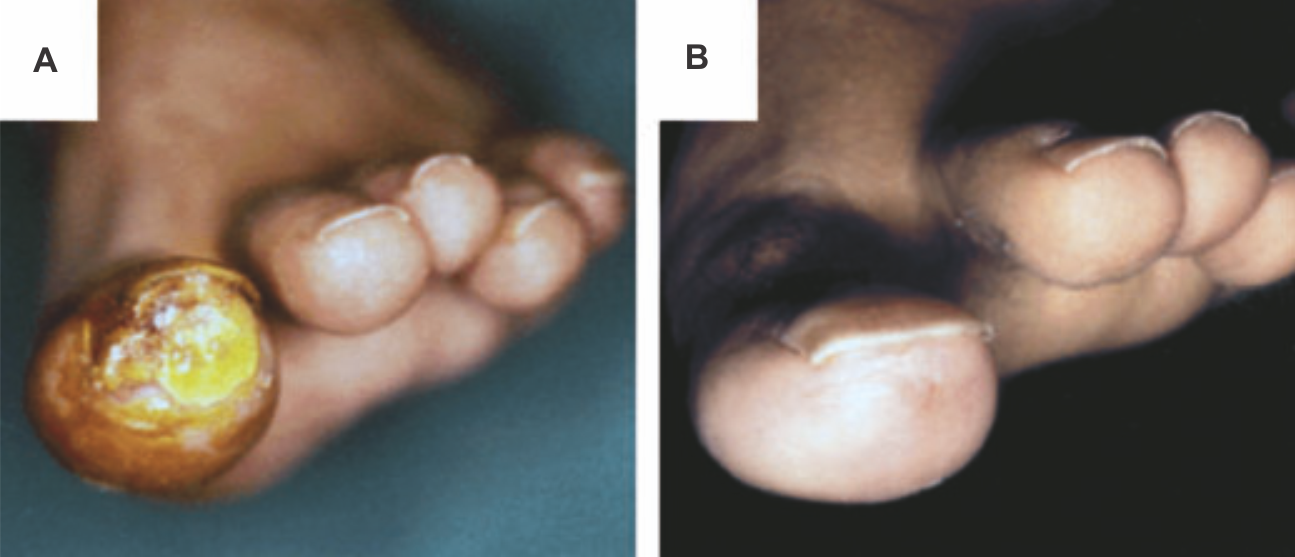
Как уже было отмечено выше, курение может усугублять течение некоторых заболеваний, способствовать канцерогенезу и потенциально ведет к зависимости. Однако, как бы это ни было парадоксально, в случае многих дерматологических заболеваний никотин показывает себя эффективным средством монотерапии. Болезнь Бюргера четко ассоциирована с курением, но ее успешно лечат при помощи жевательной резинки, содержащей никотин (Рис. 7) [106]. Вероятно, другие компоненты табака индуцируют спазм сосудов и утяжеляют течение облитерирующего тромбангиита, однако использование никотина может обладать ценным терапевтическим потенциалом. Помимо этого, ключевым компонентом лечения болезни Бюргера является отказ от курения.
Также известно о терапевтическом эффекте курения сигарет на афтозные язвы слизистой оболочки ротовой полости и гениталий при болезни Бехчета [107]. Соответствующим образом, прекращение курения ведет к появлению кожно-слизистых проявлений, особенно афтозного стоматита. Однако при лечении никотином афтозные язвы регрессируют в течение нескольких дней [108]. Механизм такого действия, вероятно, связан со способностью никотина ингибировать высвобождение провоспалительных цитокинов IL-6 и IL-8 из кератиноцитов и эндотелиальных клеток в дерме. Экстракт табачного дыма также снижает выброс IL-8, но увеличивает выработку VEGF кератиноцитами человека [109].
Воспалительные заболевания кишечника (ВЗК), по данным эпидемиологов, связаны с курением [110]. Курение и/или употребление чистого никотина может влиять на такие проявления ВЗК на слизистых оболочках и коже, как афтозный стоматит, гангренозная пиодермия и узловатая эритема. Большинство пациентов с неспецифическим язвенным колитом — некурящие либо прекратившие курение [111]. Прекращение курения усугубляет прогрессирование неспецифического язвенного колита (НЯК), но прогрессия замедляется вновь при возобновлении курения. Напротив, курящие пациенты с болезнью Крона склонны к более тяжелому течению [112]. Никотин — ключевой компонент табака, оказывающий влияние на ВЗК, ведь известно, что его введение через трансдермальные пластыри ингибирует воспаление при НЯК, чего не наблюдается при болезни Крона [113]. Интересно, что у мышей с колитом, индуцированным тринитробензол-сульфоновой кислотой, получавших анабазин — агонист нХР-α7, — повреждения тканей были менее выраженными, чем у мышей, не получавших его [114]. Никотин также применяли при лечении гангренозной пиодермии и узловатой эритемы, вероятно, ассоциированных с ВЗК, и при лечении злокачественного атрофического папулеза (т. н. болезнь Дегоса) [117], болезни Кимуры [116] и эозинофильного пустулезного фолликулита [118].
Подобно неспецифическому язвенному колиту, рецидивирующий афтозный стоматит (РАС) реже встречается у курильщиков [119]. Известно, что афтозный стоматит при резком прекращении курения также внезапно обостряется, а при возобновлении ослабевает. Заместительная терапия никотином значительно снижает частоту рецидивов РАС — вероятно, никотин можно использовать как лекарственное средство [120]. Хотя опубликованные исследования не говорят о взаимосвязи курения с красным плоским лишаем (КПЛ) слизистой оболочки ротовой полости, известен один случай КПЛ, резистентного к другим методам, который ответил на никотиновую жвачку [121].
Показано, что трансдермальный никотин напрямую снижает воспаление в коже [122]. Никотин и другие агонисты нХР могут оказывать противовоспалительное действие за счет ингибирования пролиферации лимфоцитов, эндоцитоза и фагоцитоза дендритными клетками, а также выработки АФК, супероксида и провоспалительных цитокинов [123]. Вероятно, механизм противовоспалительного действия также обусловлен противовоспалительными цитокинами, IL-10 и TGF-b, глюкокортикоидами и растворимыми рецепторами, нейтрализующими эффекты провоспалительных цитокинов. Никотин стимулирует нХР-α7, которые модулируют воспаление в отсутствие парасимпатической иннервации. Это незаменимый рецептор, необходимый для ингибирования синтеза цитокинов в ходе реализации холинергических противовоспалительных путей [124]. Наоборот, отсутствие нХР-α7 приводит к усилению провоспалительного цитокинового ответа [125].
Заключение
Табак и его компоненты влияют на кожу напрямую и опосредованно. Различные клетки кожи экспрессируют подтипы нХР, активность которых влияет на жизнеспособность клеток и их функции. Изменения в коже обусловлены как геномными, так и негеномными эффектами токсинов табака и агонистов нХР. Эффекты разнообразны: от ускорения процессов старения до мутагенеза. Эпидемиологические исследования установили как положительную, так и отрицательную взаимосвязь табакокурения с различными заболеваниями кожи. Положительная связь с определенными болезнями может благоприятно сказываться на их течении при прекращении курения, тогда как обратная — может требовать специфического лечения агонистами никотина. Важно понимать отличие действия табака и чистого никотина при болезни Бюргера. Частично противовоспалительный эффект никотина обусловлен стимуляцией нХР-α7. Эффекты компонентов табака и чистого никотина приведены в Таблице 1. Необходимы дальнейшие исследования никотинергических веществ в качестве потенциальных терапевтических агентов для некоторых кожных заболеваний.